からむこらむ
〜その220:パンと火薬と愛国者〜
まず最初に......
こんにちは。すっかり春となりましたが、皆様如何お過ごしでしょうか?
いやぁ、新年度ですね.......環境が変わった人も多いかと思いますが。
さて、今回のお話ですが。
ま、社会復帰してから毎回が「久しぶり」となりますけど(^^; その久しぶりの題材、しばらく悩んだんですがせっかくですので人物の方をメインに当てた話をしようかと思います。歴史上ではノーベル賞まで受賞した「偉大なる科学者」なのですが、実際には大きな苦労を背負い込んだ人物として知られています。
その業績は現在の生活でも大きく関連しているほどのものなのですが。
それでは「パンと火薬と愛国者」の始まり始まり.......
皆さんはノーベル賞と言う物にどういう思いがあるかは分かりませんが。
ノーベル賞を受賞した人は今までたくさんいますが、ではノーベル賞でも科学分野、つまり物理学賞や化学賞を受賞するようなほどの人物、と言うとどういうイメージがあるでしょうか?
受賞する科学者はその業績がその時々でクローズアップされ、それなりに華やかに映るでしょう。しかし実際には地道な積み重ねの成果として受賞するものであり、華やかさとはほど遠いものとなります。もちろん、彼らも人ですから中には「研究は華やかだったが人生は非常に辛いものであった」と言う人もいる。
今回はそのような人物と業績についての話題を少ししてみたいと思います。
19世紀後半から20世紀初頭にかけて猛烈な勢いで発展していった科学分野は何か?
もし、こう聞かれたらそれなりに知識のある人は「化学」と答えるでしょう。実際にこの時代、化学は猛烈な勢いで発展していき、数多くの「物質」の謎が解明されたり、あるいは登場してくる事となります。そしてこの分野において当時最も力があったのは間違いなく帝政ドイツ(プロシア)でした。実際に当時のその実力故に明治維新後の日本から数多くの科学者がドイツへと渡り、そして業績を上げています。
その代表格の一人にはエフェドリンの研究を行い、日本化学会会長および日本薬学会会頭となった長井長義がいます。
さて、この長井は1871(明治4)年から13年間ドイツでアウグスト・ホフマン(August Willhelm von Hofmann)の指導の下で研究をしています。ホフマンはモーブ(mauve)をパーキンとともに開発するなど当時のドイツの化学界を牽引する、偉大な化学者でした。
#LSDで著名なアルベルト・ホフマンとは違う人物ですのでご注意を。二人とも「A.ホフマン」ですので。
そして長井が帰国した数年後、ベルリン大学に入学してホフマン教授の講義を聴き、化学の道を志す青年がいました。
この青年の名はフリッツ・ハーバー(Fritz Haber)。彼はやがてノーベル化学賞を受賞するに至るのですが.......
フリッツ・ハーバーは1868年にシレジアのブレスラウ(現在ポーランドのブロツラウ)に生まれます。
生家は天然藍の最大の輸入業者で、裕福なドイツ系ユダヤ人。しかし母親は彼の出産で亡くなり、父親とは折りが合わずに祖母と叔母に育てられています。ちなみに彼の伯父ルードビッヒ・ハーバーは開国後の日本に領事として派遣されており、1874(明治7)年8月11日に秋田出身の尊攘派である田崎秀親に斬りつけられて死去しています。
#現在函館に遭難の碑があるそうです。
さて、フリッツですが彼自身は父親との性格の不一致があり、しかも家業を継ぐ意志がなく、成績も特に優れている訳ではありませんでした。しかしカントやゲーテ、ギリシャ文化に興味を持っており、屋根裏部屋に化学実験室を構えるほど化学にも興味を持っていました。
そしてベルリン大学に進学後の18歳の時、ホフマン教授の講義を聴いて化学の道を選ぶ事となります。
ところで、フリッツ・ハーバーを語るには重要なキーワードがいくつかあります。
彼の人生を俯瞰する上で必ず覚えておかなければならない事。それは彼は「ユダヤ人」であると言う事と、当時からドイツでは反ユダヤ主義が存在していた事です。後者は「ナチスの台頭の頃から」と思う人もいるようですが、欧州におけるユダヤ人は過去の時代から迫害の対象であり、彼の生きた時代もそのような考えが強くありました。そして、付け加えるに何よりも彼は「愛国者」でした。
ハーバーは大学で化学を修めるのですが、彼の就職はきわめて困難が伴います。
ユダヤ人である彼を迎える職場は多くなく、大学の助手のポストは全てダメ。仕様がないので故郷に帰って父親の会社のセールスマンをするも、失敗してますます仲が悪くなると言う始末。ですが彼はキリスト教に改宗するなどの順化を進め、ついに30歳の時にカールスルーエ大学に助手の地位を得ます。
その後の彼は猛烈に仕事に励み、炭化水素の研究により2年で講師に昇格。その後アニリンの製造について電気化学の研究を行い、それに伴って熱力学の研究も行い、ついには物理化学者としての地位を固めます。彼の努力は1906年に物理化学・電気化学の教授となった事で一つの成果を見る事となりました。
そして、その頃に彼は当時化学界の最も大きなテーマに取り掛かる事となります。
当時最大のテーマとは何か?
皆さんは植物の肥料として有名なものをご存知でしょうか? いわゆる「肥料の三要素」等と呼ばれる物なのですが、園芸をやっている方はご存じかもしれません。それは「窒素」「リン酸」「カリウム」でして、いずれも植物の育成に大量に必要となるものです。ですから、これを含むものを肥料として与える事は農業の必然的な流れであり、例えば糞尿はこれを多く含む為に「たい肥」として用いられる事になる。
特に窒素はたんぱく質の原料ともなるためにこの確保は重要でした。
植物は窒素をどう取り入れるか?
実はこれは単純な話ではありません。知識を持っている人は大気中の8割が窒素(N2)である事をご存知でしょうが、しかし植物はこの窒素を直接取り入れる事はできません。
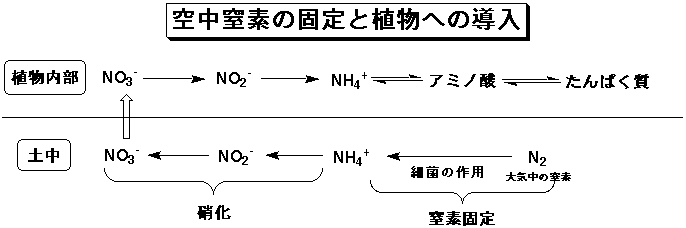
この点はかなり複雑なのですが、一つは空気中の窒素を微生物が取り込んでアンモニアを作る「窒素固定」が行われ、その後数段階の過程を経て植物に取り入れられるという系がある。つまり微生物、厳密には細菌の介在による方法があります。これは主に二つありまして、菌と植物の関係から非共生的窒素固定生物と共生的窒素固定生物と分類されています。
前者は一般的でして空気中の窒素を微生物がまずアンモニア塩(NH4+)に変換します。その後、別の微生物による「硝化」と言う過程を受ける事となります。これはアンモニア塩を土中の亜硝酸菌が亜硝酸塩(NO2-)へと酸化し、その亜硝酸塩を今度は硝酸菌が硝酸塩(NO3-)へと変化させるというものです。
この過程を経て硝酸塩(=窒素)は植物の中へ取り込まれる事となります。
一方、共生的窒素固定生物と言うものは上述とは異なり、微生物と植物で密接な共生関係によって植物が窒素を得るというものです。この菌の例としては「根粒菌(Rhizobium)」が代表格で、この細菌は土壌中に普通に存在していますがマメ科の植物と共生関係にあります(他の植物では関与しない)。この菌がマメ科の植物の根につくと「根粒(こんりゅう)」と言う粒ができ、これが空気中の窒素を取り込んでアンモニア塩にし、直接的に植物に渡すので植物はよく育つ事になります(いかにマメ科の植物にこれを共生させるかは農業上の課題になります)。
このような生物学的なプロセスがある一方、空気中の窒素が紫外線などによって酸化されて硝酸へと変化し、雨によって土中に入り込むと言うものもあります。この場合はこれを硝酸塩として植物は取りいれることとなります。もちろん、産業活動による硝酸(亜硝酸)も植物の窒素源として取り入れられる事となります。
こうして取り入れられた硝酸塩は(面倒な事に)アンモニアへと戻される事になります(還元反応)。
アンモニアに戻された後にはアミノ酸の成分として使われる事となり、これはやがてたんぱく質に変化する事になる。そして、さまざまな働き(食べられて動物のえさ、と言うのもある意味働きか)をすることとなります。
なお、植物が死んだ後、その体の窒素分はあるものは気体窒素として大気に放出され、あるいは硝酸塩やアンモニア塩となり循環します。
さて、では窒素源としての肥料はどうなのか?
当時は窒素源としては、まず石炭の乾留から副産物として得られるアンモニアがありました。これは硫酸アンモニア(硫安)として肥料にできますし(これは今でも使われる)、また酸化すれば硝酸塩をつくる事もできる。そしてもう一つは、大きな比率を占めていた南米のチリからチリ硝石(硝酸ナトリウム: NaNO3)の輸入がありました。
しかし、困った事がいくつかある。
実は19世紀ごろから硝石の枯渇の危険性が叫ばれていました。これは当時の人口の急増とそれに追いつく為の食料生産の問題に絡んでいまして、現在の石油の枯渇問題と通じるものがありました。この為に世界中でさまざまな方法が考案されたものの、いずれもコスト面などの問題から実用化しにくい。
ただ、窒素自体は大気中に無尽蔵とも言えるほどある。もし、この窒素を化合物の形で取り出せたら?
当時最も有望なアイデアは、この空気中の窒素と、石炭から得られる水素を直接化合させてアンモニアをつくる、と言う方法でした。
2 N2 + 3 H2 → 2 NH3
1904年、ハーバーはこの問題に取り掛かります。
この難問には熱力学の第三法則「絶対零度でエントロピーはゼロになる」を発見(物理化学をやるとお世話になる)し、後にノーベル化学賞を受賞する、当時ゲッチンゲン大学教授のワルター・ネルンスト(Walther Hermann Nernst)も挑んでいました。もっともネルンストはこの問題を断念するのですが、ハーバーは研究を続けて1908年に、1000℃でアンモニアが微量できたと報告します。
しかしネルンストはこの報告を見て「理論的に誤りがある」と指摘して両者は対立します。
ハーバーはこれを受けて更なる改善を行います。結果的には1909年7月に高圧炉と鉄の触媒を用いて液状のアンモニアの製造に成功する事になります。これを受けて工業化が行われる事となるのですが、それにはBASF社のカール・ボッシュ(Carl Bosch)らが引き受ける事となりました。
これはかなり危険な目に遭ったようです。有名なところでは鉄製のオートグレーブ(高温高圧の反応装置)でアンモニア合成に挑むと原料である水素が鉄を腐食し、この結果反応装置が破裂すると言う事故が発生しています。しかし最終的にはこの装置を低炭素クロムバナジウム鋼で作り、触媒を酸化鉄(Fe3O4)にアルミナ、アルカリを用いた物に改善。これでアンモニアの工業化に成功します。
この反応は200気圧、550℃と言う厳しい条件のものでした。この反応は現在「ハーバー・ボッシュ法」として知られており、現在でも使われている反応となっています。
空中窒素からのアンモニア製造の成功は非常に大きな影響を与えます。
一つは肥料の問題で、ハーバー・ボッシュ法により安定的な肥料の供給が可能となり、肥料の元となる硝石の枯渇問題や、輸入問題が一気に解決されました。
そして実はもう一つ重要な事もあります。
アンモニアの工業的製造の成功は同時にもう一つの重要な工業物資の製造につながる事となります。これは何か、と言うと実はアンモニアを酸化すると工業的に重要な硝酸(HNO3)ができます。この方法は1903年にオストワルド(Wilhelm Ostwald)によって工業化に成功したもので、白金を触媒とする「オストワルド法」として現代においても使われる方法です。
NH3 + 2 O2 → HNO3 + H2O
この硝酸、何に使うかというと実は過去に触れた通り、火薬・爆薬の製造に必要な物質となっています。つまり、今回のアンモニア製造法の確立は、同時に硝酸の大量生産へつながる事になる。硝酸ができれば当然爆薬をつくる事ができる。
時の皇帝ヴィルヘルム二世曰く「これで我が国はパンと火薬を手に入れた」とか「これで戦争ができる」とか。この話は「ありそうな作り話」と言われていますが、しかし現実にドイツはこのハーバー・ボッシュ法とオストワルド法により肥料と火薬を手に入れる事となり、この後の1914年からドイツはこの技術で第一次世界大戦を戦う事となります。
その恩恵は大きく、この方法が確立していなければドイツは戦時下の海上封鎖でチリ硝石は入手不可能のために1年と持たなかったと考えられています。
この第一次世界大戦が始まると科学者たちもそれに巻き込まれていきました。
ハーバーとアンモニア合成で競ったネルンストは、当時ベルリン大学の教授職でしたが、二人の子供を軍隊で失い、ネルンスト自身も50歳と言う齢ながら志願して自動車部隊で前線へ赴くなどします。もっとも戦局が不利になるにつれ、家族に「この戦争は負けた」と語るなど将来を冷静に分析したと言われています。ただ、あきらめずにその後は政府に請われて科学分野で協力をしています。
一方、ハーバーは愛国心に燃えて軍への協力に積極的に動きます。
もっとも、ハーバーには当初は東部戦線用のガソリン凍結防止用添加剤の選択など、あまり重要な物は回ってきませんでしたが.......ただ、彼はやがてその84で触れた通り毒ガス戦の計画・立案、実行を行う事となります。
本来は毒ガス戦の計画の中心にはネルンストがおり、彼は「相手の戦力をそぐ程度」の毒ガスの使用を考えていたものの、軍とは意見が合いませんでした。この為にネルンストは毒ガスから手を引いて火薬や迫撃砲の改良などの研究に回る事となります。
一方、愛国心に燃えてこれに臨む事となったハーバーですが、彼の毒ガス戦に対する意気込みはかなりのもので、ネルンストとは反対に「毒ガス戦により早期に戦争が終結すれば、無数の命が救えるだろう」と言う考えを持っていたようです。
彼の妻で化学者でもあったクララはこれに反対していたのですが、ハーバーは「科学者は平和時には世界に属するが、戦争時には祖国に属する」という考えからこれを受け入れませんでした。その結果、彼が東部戦線へ向かった日の夜にクララは自殺。しかしハーバーは毒ガス戦を進めるべく、彼の下で将校として働いていた 後にノーベル賞を受賞する オットー・ハーン(Otto Hahn)とともに活動しました。このときの毒ガス戦についてはもう触れませんが(興味あればイペリットの話と併せてどうぞ)、結局のところ毒ガス戦は彼の期待に反した物となります。
さらにハーバーはその著名さと、毒ガス戦の指揮者と言う事から各方面から大いに恨まれる事となりました。事実ドイツの敗戦後、フリッツ・ハーバーは「戦争犯罪人」の候補として名が挙げられてしまう事になります。
ハーバーとしては盲目的なまでの「愛国心」でもって毒ガスを使用し、また愛国心を訴えて各方面からの協力を 実際にエミール・フィッシャーなどそうそうたる面々が知恵を貸している 得て戦争の遂行を協力しています。ですが結果的にはひたすらに戦争を伸ばし、犠牲者を増やした。また毒ガス戦は国際法の違反となる行為でもあった為に(「フランスが先だった」など言い訳は色々ありましたが)多くの人はハーバーが戦争犯罪人として国際法廷で処刑されるだろう、と予想していました。
このときのハーバーは脳下垂体の病気と相まって相当なストレスに悩まされており、友人から「75%死人だった」と評されるほどの状態だったと言われています。
ただ、これを救った物がありました。
戦争の休戦から2ヶ月たった1918年の暮れ。絶望の底にあったハーバーに対し、ノーベル化学賞を授賞するとの発表が行われます。それまで誰も成し遂げなかった空中窒素からのアンモニアの合成法の確立......確かにこれは大きな意義を持つものであり、十分にノーベル賞を受ける資格が彼にはありました。無論、ここら辺は政治的状況も鑑みたものもあったと思われますが(敗戦後日本に湯川秀樹のノーベル賞と同様のインパクトはあったでしょう)。
この発表は連合国側から非難を受けます。ですが、ハーバーの業績その物は確かに重大なものであり、さらに人類への貢献となる。結局、ノーベル賞委員会はこれら非難を一蹴します。これにより休戦と同時に人目を避けていたハーバーは久しぶりに表舞台へ登場し、ノーベル賞を受賞する事となりました。
ハーバーはこのような事から最終的に社会、と言うより科学界に復帰します。
一方、彼の愛したドイツはベルサイユ条約により徹底的に解体されてしまい、またドイツ化学工業界も危なくなります。しかしボッシュは化学工業技術や軍需工場の解体に対して抵抗し、これに成功します。その後も紆余曲折を経て、ボッシュなどの活躍からドイツの化学工業界は徐々に回復。
そしてボッシュは1925年にはドイツのほとんどの化学工業を傘下に収める(従業員数13万人と言われています)I・G・ファルベンの会長に就任し、これでドイツ化学工業は不死鳥のごとき復活を遂げる事となります。
この間ハーバーは1924(大正13)年に世界一周の旅にでかけています。西廻りでチリを避けた(ハーバー・ボッシュ法によりチリ硝石が売れなくなったので)ものでしたが、日本にも「技術指導」のために2ヶ月滞在。この間に函館で伯父の遭難50周年の追悼式にでるなどしています。
また、ドイツでも物理化学研究所で研究を再開しています。
その活動の一つには、ベルサイユ条約で莫大な量の負債を負う事となった祖国ドイツの為、海水から金を回収しようと言う試みを行っています。当時の推計で海水1t当たり数mgの金が含まれているだろうと言う話があり、ハーバーはこの金を回収して賠償金に充てる事を提案して実験を行います。
もっともハンブルグ〜ニューヨーク間で実際に回収してみたところ、実際には海水1tあたり0.04mgと言うレベルでお話にならないと言う事が発覚し、結局1928年(このとき彼は60歳)にこれは無しになりますが。
そして1920年代も半ばを超える頃、ドイツでは失業者が多かったものの世情もある程度安定をしていました。
科学界も復活して研究も進むのですが、ちょうどこの頃ラザフォードの研究などから核物理学が始まりヨーロッパではこの研究が活発に行われる事となります。ドイツでもこの流れに乗って核物理学が活発になり、ハーンを始め、ユダヤ人女性でオーストリア人のリーゼ・マイトナーなどが活躍しています。
ところが1929年10月24日、通称「魔の木曜日」に端を発した世界大恐慌が世界はもちろんの事、ドイツの世情を不安定にしていきます。
大恐慌後、ドイツの世情不安は深刻となりこの中でナチスが徐々に台頭してくる事となります。大恐慌前に10席をわずかに上回るだけの勢力でしかなかったナチスは伸張して1933年にヒトラーが政権を掌握。そしてユダヤ人の追放が開始される事となりました。
無論、ナチスに対抗する科学者もいまして、ボッシュ(1931年にハーバー・ボッシュ法の確立によりノーベル化学賞を受賞しています)やネルンストなどはこの流れに抵抗しました。ボッシュは直にヒトラーと面談してユダヤ系の科学者の追放を「ドイツから物理や化学を追放する事と同じ」と直訴するのですが、ヒトラーはこれに対し「それなら、これから百年はドイツでは物理や化学無しでやっていこうではないか」と放言。ナチスによるユダヤ人パージは進められ、政権掌握後には次々と職場から追放されるユダヤ人が増えます。
愛国者であっても「ユダヤ人」であるハーバーもこの追放劇に巻き込まれる事となります。実際、彼は教育大臣に抗議の手紙を書いて研究所を辞める事となります。
#なお、ユダヤ系オーストリア人であったマイトナーはナチスのオーストリア併合によってナチスの排斥の対象となり、スウェーデンに脱出しています。
ハーバーはその後、健康を害してスイスのサナトリウムに療養へ出ます。
その後、イギリスでラザフォードらが手を尽くしてドイツからのユダヤ系科学者の亡命を受け入れるのですが、ハーバーもまた招かれてイギリスへ亡命する事となります。しかし第一次世界大戦で毒ガス戦の立て役者であったハーバーへの風当たりは強く、またイギリスの冬の寒さに身体が堪えた為にスイスのバーゼルへと保養旅行へ向かいます。
そして1934年1月29日、故国を目の前にしたバーゼルで冠状動脈硬化症により、睡眠中に死去します。愛国者にしてノーベル賞を受けるほどの業績を残した科学者は、このようにして故国に裏切られてこの世を去っていきました。
この報を聞いた在ドイツの心ある科学者たちは、1935年に追悼式を行います。当然ナチスの妨害が入る訳ですが、ボッシュはI・G・ファルベンの従業員を引き連れて追悼式に参加。演説はハーンが行いました。
その後、ボッシュはナチスとの軋轢もあり引退し、1939年のナチスによるポーランド侵攻の直後に「負け戦」を予想して死去。オットー・ハーンはこの前年に核分裂を発見(ハーンはこの為に1944年にノーベル化学賞を受賞)し、これを元にアメリカは原爆の開発に成功。この中核にはアメリカへと脱出した大勢のユダヤ系の科学者が関与していました。
ナチスは自らの首を絞める事となります。
#ハーンの核分裂の発見は注釈が必要でしょう。
#ドイツのカイザー・ウィルヘルム研究所時代からハーンは実験を、マイトナーは理論や意味を受け持っていました。ハーンは実験結果を亡命中のマイトナーに手紙を出して解釈を頼み、マイトナーがこれを明確にしています。現在は両名をもって核分裂の発見者として扱われています。ただし、マイトナーはノーベル賞を受賞していません。
さて、以上がフリッツ・ハーバーの話です。
彼自身の人生は客観的に見て幸福に満ちたものだったとは言えません。愛国者ゆえに、ユダヤ人ゆえに、また才能があったゆえに起こった悲劇と言うものかもしれませんが、しかしノーベル賞の本懐である「人類への貢献」と言う点では彼は実際に、極めて大きな業績を残したといえます。
我々は実際に現在に至るまでその成果(本文にはありませんが、ガラス電極を発明したのもハーバー)を利用している訳ですから。
ですが「愛国者」であった彼が今のドイツを見たらどう思うかに興味はあります。ただ、彼の生き様は「科学」と「愛国者」と言うものの関係を考えさせられるものではあるかと思います。
もっとも、いつの時代にもつきまとうものだと思いますが。
では長くなりました。
今回は以上という事にしましょう。
さて、今回の「からむこらむ」は如何だったでしょうか?
色々と時間もない中なのですが(^^; とりあえず以前から少し考えていたネタをやってみました。ま、ドイツの化学工業で最も輝き、そして目立ったものの祖国に裏切られた、と言う意味で名を残す科学者の物語ですが。ノーベル賞を受賞する人が必ずしも幸福である事ではない、と言う事。そして時代の流れに翻弄された時代であったという事。
理解していただければと思います。
そういう事で、今回は以上ですが。
次回は......いつになるんだか(^^; 話のネタがあっても仕事で熟成させる時間がないんですよねぇ.......と言う事で、また気楽にお待ちくださいませ(^^; もっとも、感想はいつでも歓迎いたしますがね。
そう言うことで、今回は以上です。
御感想、お待ちしていますm(__)m
次回をお楽しみに.......
(2005/04/11公開)
前回分 次回分
からむこらむトップへ

